Papovaviiruse Selgitus: Pähiklaste, Mõju ja Käimasolev Võitlus Viirusnakkuste Vastu. Uuri, Kuidas See Viiruseliik Kujundab Kaasaegset Meditsiini.
- Sissejuhatus Papovaviirusesse: Ajalugu ja Klassifikatsioon
- Papovaviiruse Struktuur ja Geneetiline Koostis
- Ülekandeteed ja Peremeeste Spekter
- Papovaviirusega Seotud Haigused
- Diagnostikatooted ja Tuletamine
- Praegused Ravi- ja Ennetamisstrateegiad
- Papovaviirus Uuringutes: Edusammud ja Tuleviku Suunad
- Allikad ja Viidatud Materjal
Sissejuhatus Papovaviirusesse: Ajalugu ja Klassifikatsioon
T termin “Papovaviirus” viitab ajalooliselt rühmale väikestele, kattepuudulikele DNA viirustele, mis liideti algselt ühiste struktuuri- ja geneetiliste omaduste põhjal. Nimi “Papovaviirus” on akronüüm kolmest prototüüviirusest: PApilloom, POlioom ja VAkuoleeriv viirus (simiaalse viirus 40, SV40). Need viirused avastati esmakordselt 20. sajandi keskel loomade kasvajate ja viirusliku onkogeneesi uuringute ajal, mis tõi kaasa olulisi edusamme viiruslike vähi põhjuste ja molekulaarbioloogia mõistmisel. Varased uuringud näitasid, et selle rühma liikmed võivad loomadel käivitada kasvajaid, tekitades huvi nende võimaliku rolli üle inimvähi korral ja nende kasulikkuse üle rakkude transformatsiooni ja geenide reguleerimise uurimise mudelsüsteemidena Riiklik Biotehnoloogia Informatika Keskus.
1999. aastal viis molekulaarviroloogia ja filogeneetiline analüüs Papovaviridae perekonna ümberklassifitseerimiseni kaheks eraldi perekonnaks: Polyomaviridae ja Papillomaviridae, nagu tunnustas Rahvusvaheline Viiruste Taksonoomia Ühendus (ICTV). See reorganiseerimine põhines genome korralduse, paljunemisstrateegiate ja peremeeste spektri erinevustel. Polyomaviiruseid ja papillomaviiruseid uuritakse nüüd kui eraldi entiteete, millel on igaühel ainulaadne kliiniline ja bioloogiline tähendus. Hoolimata termini “Papovaviirus” aegumisest praeguses taksonoomias, on selle ajalooline kontekst oluline viroloogia evolutsiooni ja DNA tuumaviiruste klassifitseerimise mõistmiseks.
Papovaviiruse Struktuur ja Geneetiline Koostis
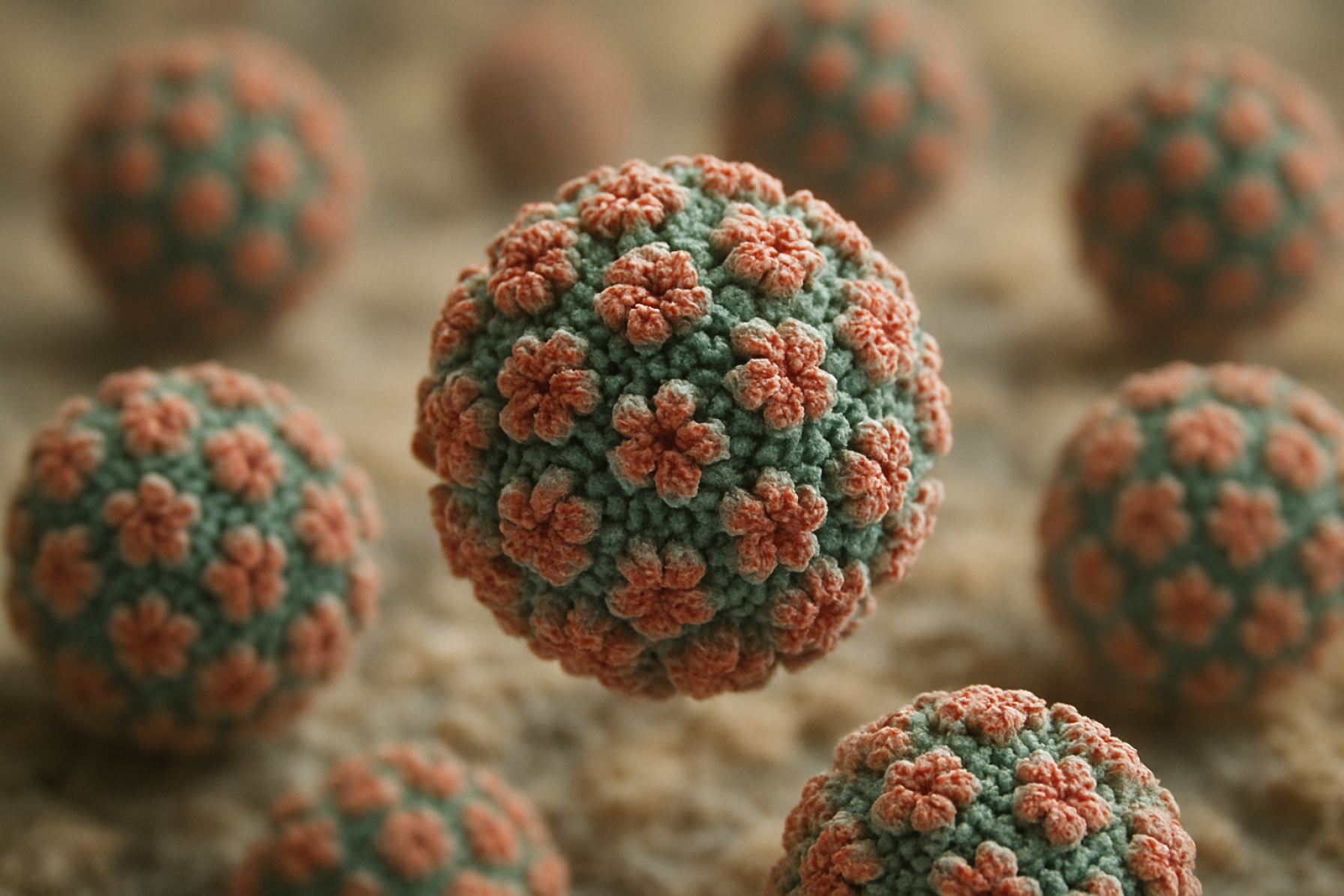
Papovaviirused on kattepuudulikud, ikoosahedraalsed viirused, mille diameeter on umbes 40–55 nm. Nende kapsiid koosneb 72 kapsomäärast, pakkudes struktuurilist stabiilsust ja vastupidavust keskkonnateguritele. Viiruslik genome koosneb ringikujulisest, kaheahelalisest DNA molekulist, mis tavaliselt ulatub 5,000 kuni 8,000 aluspaari pikkuseks. See genome on tihedalt seotud rakuliste histoonidega, moodustades virioni sees mini-kromosoomi sarnase struktuuri, mis on haruldane DNA viiruste seas ja aitab kaasa viiruslike geenide ekspressiooni reguleerimisele.
Papovaviiruste geneetiline korraldus on suhteliselt kompaktne, kus on kattuvad lugemisraamid ja multifunktsionaalsed reguleerimispiirkonnad. Genome jaguneb varajasteks ja hilisteks piirkondadeks. Varajane piirkond kodeerib viiruslikke paljunemiseks ja peremeesrakutsüklite reguleerimiseks vajalikke valke, nagu suured T-antigeenid polyomaviirustes ja E6/E7 valkudel papillomaviirustes. Hiline piirkond kodeerib struktuurivalke, peamiselt peamisi ja väikeseid kapsiidivalke (nt VP1, VP2 ja VP3 polyomaviirustes; L1 ja L2 papillomaviirustes), mis on hädavajalikud virioni kokkupanekuks ja nakkusvõimeks.
Papovaviirused paljunevad peremeesrakku tuumas, kasutades genome paljundamiseks peremehe DNA polümeraase. Nende ainulaadsed geneetilised ja struktuurilised omadused on olnud ulatuslikuks uurimiseks, pakkudes teadmisi viiruslikust onkogeneesist ja viirusel põhinevate geeniteraapia vektorite arendamisest. Täiendavateks detailideks papovaviiruste struktuuri ja geneetika kohta viidake Haiguste Tõrje ja Ennetamise Keskuse ja Riiklik Biotehnoloogia Informatika Keskus.
Ülekandeteed ja Peremeeste Spekter
Papovaviirused, mis ajalooliselt hõlmasid perekondi Papillomaviridae ja Polyomaviridae, näitavad mitmekesiseid ülekandeteid ja laia peremeestespetsiifilisust. Ülekanne toimub tavaliselt otsese kontakti kaudu nakatunud kudede, kehavedelike või saastunud pindadega. Näiteks inimeste papilloomiviirused (HPV-d) levivad peamiselt naha-kontakti või seksuaalkontakti kaudu, samas kui polyomaviirused nagu BK ja JC viirus levivad sageli hingamisteede tilkade, uriini või saastunud veepunktide kaudu. Vertikaalse ülekande juhtumid emalt lapsele on samuti dokumenteeritud teatud polyomaviiruste, sealhulgas puhul Haiguste Tõrje ja Ennetamise Keskus.
Papovaviiruste peremeeste spekter on lai, nakatades erinevaid selgroogsete liike. HPV-d on tugevalt liigispetsiifilised, peamiselt nakatades inimesi, samas kui polyomaviirused võivad nakatada laiemat valikut imetajatest ja lindudest. Peremehe nakatumise spetsiifilisus sõltub peamiselt viiruslike kapsiidivalkude ja peremeesrakku pinna retseptorite vahelisest interaktsioonist, mis mõjutab koetropismi ja haiguse avaldumist. Erakordselt on mõned loomade polyomaviirused, nagu simiaalse viirus 40 (SV40), uuritud nende võime tõttu ületada liigipiire katsetingimustes, tekitades muret zoonoosi potentsiaali üle Riiklik Biotehnoloogia Informatika Keskus.
Papovaviiruste keskkonnastabiilsus hõlbustab nende ülekannet, kuna need kattepuudulikke viirused suudavad pindadel püsida pikema aja. See vastupidavus rõhutab hügieeni ja desinfektsiooni tähtsust leviku ennetamisel, eriti tervishoiu ja ühiskondlikes keskkondades. Papovaviiruste ülekande dünaamika ja peremehe spetsiifilisuse mõistmine on kriitilise tähtsusega tõhusate rahvatervise sekkumiste arendamiseks ja seotud haiguste kontrollimiseks.
Papovaviirusega Seotud Haigused
Papovaviirused, mis klassifitseeritakse ajalooliselt väikeste, kattepuudulike DNA viiruste rühmaks, jagunevad nüüd kaheks peamiseks rühmaks: Papillomaviridae ja Polyomaviridae. Need viirused on seotud mitmete haigustega inimestes ja loomades, peamiselt mõjutades epiteeli ja närvikudesid. Kõige kliiniliselt olulisemad haigused, mis on seotud papovaviirustega, on põhjustatud inimeste papilloomiviirustest (HPV-d) ja inimeste polyomaviirustest.
HPV-d on tuntud oma rolli poolest healoomuliste ja pahaloomuliste kahjustuste kujunemisel. Madala riskiga HPV tüübid on vastutavad tavaliste tüükade ja suguelundite tüükade eest, samas kui kõrge riskiga tüübid, nagu HPV-16 ja HPV-18, on etioloogiliselt seotud emakakaelavähiga ja teiste anogenitaalsete ja orofarüngeaalsed vähkidega. Nende viiruste onkogeensed omadused on seotud nende võimega integreerida peremehe genoomi ja häirida rakutsükli reguleerimist, mis viib pahaloomulise transformatsioonini Haiguste Tõrje ja Ennetamise Keskus.
Polyomaviirused, sealhulgas BK viirus ja JC viirus, on immunokompetentsetes isikutel tavaliselt asümptomaatilised, kuid võivad immuunpuudulikkuse korral põhjustada tõsist haigust. BK viirus on seotud neeruhaiguse ja hemorraagilise tsüstiidiga, eriti neerusiirdamise saajate seas, samas kui JC viirus on progresseeruva multifokaalse leukotsüloosi (PML) põhjustaja, kesknärvisüsteemi demüeliniseeriv haigus, mida täheldatakse kaugelearenenud immunosupressiooniga patsientidel Haiguste Tõrje ja Ennetamise Keskus.
Kokkuvõttes on papovaviirused seotud ulatusliku haiguste spektriga, ulatudes healoomulistest proliferatiivsetest kahjustustest kuni eluohtlike pahaloomuliste haiguste ja neuroloogiliste häireteni, rõhutades nende olulist mõju rahvatervisele.
Diagnostikatooted ja Tuletamine
Papovaviiruste, kuhu kuuluvad Polyomaviridae ja Papillomaviridae perekonnad, tuvastamise diagnostikatooted on molekulaari bioloogia edusammude tõttu oluliselt arenenud. Traditsiooniline tuvastamine tugines histopatoloogilisele uurimisele, kus iseloomulikud tsütopaatilised efektid, nagu koilotsütoos epiteelirakkudes, viitasid papillomaviiruse nakkusele. Kuid need meetodid puuduvad spetsiifilisus ja tundlikkus, eriti latentsete või subkliiniliste nakkuste korral.
Praegu on molekulaartooted papillomaviiruste tuvastamiseks kuldstandardiks. Polümeraasiketiga reaktsiooni (PCR) katsed on laialdaselt kasutusel nende kõrge tundlikkuse ja spetsiifilisuse tõttu. PCR suudab tuvastada viiruslikku DNA-d kudede biopsiides, tampoonides või kehavedelikes ja seda saab kohandada, et tuvastada spetsiifilisi viiruslikke genotüüpe, mis on olulised epidemioloogiliste uuringute jaoks ja kõrge riskiga inimese papilloomiviiruse (HPV) tüüpide kindlakstegemiseks. Reaalajas kvantitatiivne PCR (qPCR) võimaldab samuti viiruskoormuse kvantifitseerimist, mis võib olla oluline haigusprotsessi jälgimisel või ravivastuse hindamisel Haiguste Tõrje ja Ennetamise Keskus.
Lisaks PCR-ile võimaldavad in situ hübriidmoodused lokaliseerida viiruslikke nukleiinhappeid kudede lõikudes, pakkudes nii diagnostilisi kui ka teadusuuringute väärtusi. Seroloogilised katsed, nagu ensüümidega seotud immunosorbentskatsetele (ELISA), kasutatakse viiruslike valkude vastu tekkinud antikehade tuvastamiseks, mis viitab varasemale või käimasolevale nakkusele, kuigi need ei ole ägeda diagnoosi jaoks vähem kasulikud antikehade vastuse viibimise tõttu Maailma Terviseorganisatsioon.
Uued tehnoloogiad, sealhulgas järgmise põlvkonna sekveneerimine (NGS), pakuvad põhjalikku tuvastamist ja genotüüpimist papovaviiruste osas, soodustades uute tüvede ja kaainfektsioonide avastamist. Need arenenud meetodid on üha olulisemad seire, vaktsiinide arendamise ja papovaviirusega seotud haiguste patogeneesi mõistmiseks.
Praegused Ravi- ja Ennetamisstrateegiad
Praegused ravimeetodid ja ennetamisstrateegiad papovaviiruse nakkuste, mille hulka kuuluvad peamiselt inimeste papilloomiviirus (HPV) ja polyomaviirused, keskenduvad terapeutilistele ja profülaktilistele lähenemistele. HPV jaoks, mis on seotud emakakaela ja teiste anogenitaalsete vähkidega, samuti orofarüngeaalsed vähkidega, on kõige tõhusam ennetav meede vaktsineerimine. Profülaktilised vaktsiinid nagu Gardasil 9 ja Cervarix suunavad kõige onkogeensemaid HPV tüüpe ja on tõestanud kõrget efektiivsust nakatumise ja sellele järgnenud vähieelsete kahjustuste arengu ennetamisel, kui neid manustatakse enne kokkupuudet Haiguste Tõrje ja Ennetamise Keskus. Adolescente sihitud vaktsineerimisprogrammid on viinud HPV esinemissageduse ja seotud haiguste olulise vähenemiseni paljudes riikides.
Inimestel, kes on juba HPV-d nakatunud, ei ole praegu viirusvastaseid ravimeid, mis otseselt viirust elimineeriks. Ravi keskendub kliiniliste avalduste ravimisele, nagu tüügaste eemaldamine krüoteraapia, kirurgilise ekstsisiooniga või kohalike ainete, nagu imikimood ja podofüllotoksiin Maailma Terviseorganisatsioon. Kõrge astme emakakaelavigastuste puhul on tavalised ekstsisioonsed protseduurid, nagu silmus elektrooperatiivne ekstsisioonsüsteem (LEEP).
Polyomaviiruse nakkused, nagu BK ja JC viirus, on eriti probleemsed immuunpuudulikkuse korral. Need nakkused ei ole spetsiifilised viirusvastased ravimid heaks kiidetud; juhtimine on suuresti toetav, vähendades immunosupressiooni, mis on peamine strateegia siirdamise saajate seas UpToDate. Sihtmärgiks mõeldud viirusvastaste ja immunoteraapiate uurimine on jätkuvas etapis, kuid praegu tugineb ennetamine hoolikale jälgimisele ja varajasele sekkumisele.
Papovaviirus Uuringutes: Edusammud ja Tuleviku Suunad
Papovaviirused, mis ajalooliselt hõlmasid Polyomaviridae ja Papillomaviridae peresid, on olnud viroloogia uurimises olulised tänu nende ainulaadsetele paljunemisprotsessidele ja onkogeenetele potentsiaalile. Viimased edusammud molekulaarbioloogias ja genoomikas on oluliselt laiendanud meie arusaamist papovaviiruse bioloogiast, eriti viiruse ja peremehe interaktsioonide, viirusliku onkogeneesi ja immuunpõgenemise strateegiate kontekstis. Suur tõhusus ja CRISPR-põhised geeni redigeerimise meetodid on võimaldanud teadlastel viirusgenoomi lahti harutada ja tuvastada kriitilisi reguleerivaid elemente, mis on seotud rakumuutumise ja püsivuse Riiklik Biotehnoloogia Informatika Keskus.
Vähiuuringutes on inimeste papillomaviiruste (HPV-d) roll emakakaelavähi ja muude anogenitaalsete vähkide korral toodud esile profülaktiliste vaktsiinide arendamisel, mis on näidanud silmapaistvat efektiivsust HPV-dest tingitud onkoloogiliste haiguste vähendamisel Haiguste Tõrje ja Ennetamise Keskus. Samuti on uuringud polyomaviiruste, nagu BK ja JC viirus, andnud ülevaate viiruslikust latentsusest ja reaktiivimisest, eriti immunokompetentsete isikute seas Riiklik Vähikeskus.
Tulevikujõudud, uurimisseeritud uute viirusvastaste ravimeetodite, täiustatud diagnostikavahendite ja järgmise põlvkonna vaktsiinide arendamine, mis sihivad laiemat spektrit papovaviiruse tüüpe. Lisaks, viirustüüpi osakesten (VLP) uurimine kui vaktsiini platvormide ja viiruslike mikroRNA-d uurimine patogeneesina esindab paljutõotavaid tulevikusuundi. Need saavutused mitte ainult ei suurenda meie arusaamist papovaviirustest, vaid aitavad ka kaasa laiematele rakendustele vähi ennetamises ja raviuuenduses Maailma Terviseorganisatsioon.
Allikad ja Viidatud Materjal
- Riiklik Biotehnoloogia Informatika Keskus
- Polyomaviridae
- Haiguste Tõrje ja Ennetamise Keskus
- Maailma Terviseorganisatsioon
- UpToDate
- Riiklik Vähikeskus